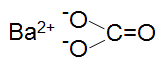 BaCO3
BaCO3
A bárium szénsavval alkotott sója.
bárium-karbonát
(witherit)
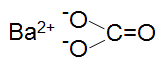 BaCO3
BaCO3
A bárium szénsavval alkotott sója.
 Előfordulás
Előfordulás
A természetben a rombos
kristályrácsú witherit nevű ásvány formájában (a képen) megtalálható.
Fizikai és kémiai tulajdonságok:
Fehér, szilárd anyag.
Sűrűsége 4,438 g/cm3
Vízben nem oldódik.
Hevítve (1300°C körül) bárium-oxidra és szén-dioxidra
bomlik:
BaCO3 -> BaO2 + CO2
Szénsavas vízben, bárium-hidrogén-karbonáttá alakul:
BaCO3 + H2CO3 -> Ba(HCO3)2
Híg sósavval (vagy salétromsavval) szén-dioxid keletkezésével reagál:
BaCO3 + HCl -> BaCl2 + H2O+ CO2
Előállítás
Báriumsók lúgos karbonátoldattal történő reakciójával,
például bárium-kloridból szódával:
BaCl2 + NaCO3 -> BaCO3 + 2 NaCl
Iparilag bárium-szulfid és szén-dioxid reakciójával:
BaS + CO2 + H2O -> BaCO3 + H2S
Felhasználás
Más báriumsók előállításának nyersanyagaként
Kerámiák gyártásakor folyósítószerként
Egyes optikai üvegek gyártásához nyersanyagként.
Pirotechnikai keverékekben (zöld) lángfestésre.
Régebben rágcsálóírtó szerként is alkalmazták.
Biológia
Mérgező hatású, a gyomorsav feloldja.
Gyomor- és bélpanaszokat, görcsöket, izombénulást okozhat.