 Az elsőnek,
1870 - 90 körül, kifejlesztett szárazelem típus.
Az elsőnek,
1870 - 90 körül, kifejlesztett szárazelem típus.Leclanche vagy szén-cink szárazelem
(cink-klorid elem, cink-klorid-cella)
 Az elsőnek,
1870 - 90 körül, kifejlesztett szárazelem típus.
Az elsőnek,
1870 - 90 körül, kifejlesztett szárazelem típus.
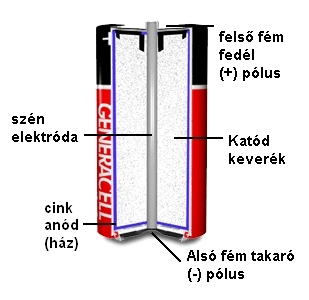
A szén-cink szárazelemek felépítése az ábrán látható.
Tulajdonságok
Feszültség:
1,5 volt (cellánként).
Anód: cink
(Zn) (a henger alakú tartály)
Katód: mangán-dioxid
(MnO2), mint depolarizátor, egy szénrúddal
a közepén. (A jobb vezetőképesség érdekében szénport
is kevernek hozzá.)
Elektrolit:
ammónium-klorid vagy a cink- klorid elemekben (cink-klorid-cella) cink-klorid
oldat. A "száraz"elem
változatban (az ábrán) egy semleges fém-oxidba
"felitatott" gél (cink-klorid paszta) formájában.
Az oldódó cinkatomok elektron leadás után pozitív cink ionokként jutnak az oldatba, miközben elektronjaikat a cinklemezen hagyják. Ennek hatására negatív töltés halmozódik fel a cinklemezen, ezért ennek az elemnek cink a negatív kivezetése. A kémiai folyamat addig tart, amíg el nem fogy a cink (kilyukad a tartály), vagy ki nem szárad az oldat.
Az áramtermelő elektrokémiai folyamat teljes rekciója, az elektrolittól függően, az alábbi:
Zn + 2MnO2 +2NH4Cl -> 2MnOOH + Zn(NH3)2Cl2
Zn + 2MnO2 + 2H2O + ZnCl2 -> 2MnOOH + 2 Zn(OH)Cl
Elméleti energiasűrűségük
150 Wh/kg, a gyakorlatban ennek kb. fele.
A szén-cink elemek aránylag olcsók.
 Alkalmazás
Alkalmazás
Hosszú időn keresztül "egyeduralkodó" volt az elektronikai eszközök
áramforrásaként.
Kisebb fogyasztású eszközökben ma is elterjedt.
Az elektromos áramot termelő elektrokémiai folyamatokat bemutató animációk találhatók a Kémia rész galvánelem címszavánál.
Öveges tanár úr szemléletesen
foglakozik a szén-cink szárazelemekkel a Fizika blokk Hogyan működik a galvánelem? című részében.