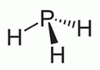
 PH3, a foszfor hidridje
PH3, a foszfor hidridjefoszfin
(foszfor-hidrogén, difoszfin, difoszfán)
Előfordulás
A természetben is előfordul, mint foszfortartalmú fehérjék rothadási terméke.
Előállítás
Foszfidokból vízzel:
Ca3P2 + H2O = 2 PH3 + 3 Ca(OH)2
Tömény alkálilúg oldja a színtelen foszfort, alkáli-hipofoszfit és foszfin keletkezik:
P3 + 3 KOH + 3 H2O = PH3 + 3 KH2PO2
Ennél a folyamatnál mellékreakcióval kevés difoszfin /difoszfán/ (P2H4) is keletkezik, amely levegőn azonnal meggyulladó, színtelen folyadék.
Fizikai és kémiai tulajdonságok
Fokhagyma szagú gáz.
Forráspont: -87,7°C
Olvadáspont: -133°C
Sűrűség: a levegő
1,17-szerese, folyadékként 0,8 g/cm3
Erős redukálószer.
Hevítve, illetve égésekor bomlik. Égésekor foszfor-oxidok keletkeznek.
Hevesen reagál levegővel, oxigénnel, oxidáló szerekkel, például a nitrogén-oxidokkal,
fémek nitrátjaival, halogénekkel.
Vízben oldódik: 26ml/100 ml, 17°C-on.
Felhasználás
Kémiai szintézisek alapanyaga.
Biológia
Belélegezve köhögés, hányingert, égő érzést, szédülést, mellkasi fájdalmat és
szorításérzést, reszketést, légszomjat okozhat..