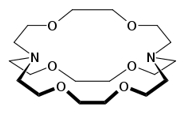
kriptandok
([2,2,2]-kriptand, Kryptofix)
Különböző kationokat megkötni képes biciklusos és policiklusos többfogú ligandumok.
A crypt az elnevezésben azt jelenti, hogy képesek ligandumokat "kriptába" zárni.
Történet
1987-ben Donald J. Cram, Jean-Marie Lehn és Charles J. Pedersen kémiai Nobel-díjat kaptak a kriptandok és a koronaéterek felfedezéséért és meghatározásáért, megteremtve ezzel a szupramolekuláris kémia gyümölcsöző területét.
Szerkezet
A leggyakoribb és legfontosabb kriptand az
N[CH2CH2OCH2CH2OCH2CH2]3N
IUPAC neve 1,10-diaza-4,7,13,16,21,24-hexaoxobiciklo[8.8.8 ]hexakozán. Közismertebb néven [2,2,2]-kriptand.
A szögletes zárójelben lévő a két nitrogénkötés közötti oxigénatomokat és ezáltal a kötőhelyek számát jelölik.
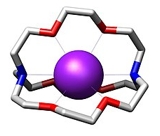
A [2,2,2]-kriptand szerkezeti képlete és molekulaképe (egy káliumionnal)


Felhasználás
Számos kriptand kereskedelmileg elérhető Kryptofix márkanéven.
Alkalmazzák szervetlen és fémorganikus sók előállításánál reagensként.
Bár előállításuk a koronaéterekénél drágább, de jobban megkötik az alkálifém kationokat és szerves oldószerekben oldhatóvá teszik azokat.