 H2CO3
H2CO3
A szén-dioxid (CO2) vízzel történő reakciójával keletkező gyenge sav (a reakció egyenletét lásd lentebb).
szénsav
(szódavíz, szikvíz)
 H2CO3
H2CO3
A szén-dioxid (CO2)
vízzel történő reakciójával
keletkező gyenge sav (a reakció egyenletét
lásd lentebb).
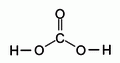
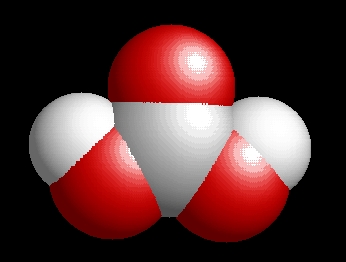
A szénsav molekulaképe balra golyó és pálcika jobbra térkitöltéses megjelenítésben.

|
|
A Szensav.pdb koordináta fájl térben megjeleníthető a https://sourceforge.net/projects/openrasmol/ címről letölthető molekulamegjelenítő programmal
Fizikai és kémiai tulajdonságok
Gyenge sav.
Sói a karbonátok,
savanyú sói a hidrogén-karbonátok (vagy
bikarbonátok).
Két lépésben disszociál, bikarbonát-
(HCO3-) és karbonát-
(CO32-) ionokat eredményezve.
A természetes vizek általában telítettek a légkörből
származó szén-dioxiddal,
és pH-értéküket a jelenlévő bikarbonát-
és karbonátionok mennyisége határozza
meg.
A tiszta szénsavat tartalmazó esővíz pH-értéke
kb. 5.
Keletkezés
A szén-dioxid (CO2)
vízben történő oldódásával,
megfordítható reakcióban:
CO2 + H2O <-> H2CO3
Felhasználás
 Szénsavat
tartalmaznak a legnépszerűbb üdítő italok, ásványvizek, sör, pezsgő, stb.
Szénsavat
tartalmaznak a legnépszerűbb üdítő italok, ásványvizek, sör, pezsgő, stb.
Az alkoholos erjedés során cukorból az
alkohol mellett szén-dioxid
is keletkezik, ami vízzel
reakcióba lépve szénsavat ad. Ilyen módon kerül szénsav pl. a
sörbe és a pezsgőbe.
Az üdítő italokat, és általában az ásványvizeket is, mesterségesen dúsítják
szén-dioxiddal.
Nyomás csökkenés esetén (a palackot kinyitva)
a szénsav lassan szén-dioxidra
és vízre bomlik,
ez okozza a buborékképződést (lásd a fentebbi reakciót).
Talán kevésbé ismert, hogy Jedlik Ányos
kezdett el előszőr szódavizet (szikvizet) készíteni, és készített
ehhez megfelelő gépet (1849-ben). Vagyis ő kezdett el mesterségesenvizet szénsavval dúsítani .