aldehidek
(aldehidcsoport)
 Ha egy szénhidrogén
szélső szénatomján két hidrogént hidroxilgyökkel
helyettesítünk, akkor a keletkező geminális kétértékű alkoholok
nem állandóak, hanem víz lehasadásával aldehidekké
alakulnak, ezekben végső helyzetű -HC=O gyök
van.
Ha egy szénhidrogén
szélső szénatomján két hidrogént hidroxilgyökkel
helyettesítünk, akkor a keletkező geminális kétértékű alkoholok
nem állandóak, hanem víz lehasadásával aldehidekké
alakulnak, ezekben végső helyzetű -HC=O gyök
van.
Az aldehidcsoport elektronvisszatartó csoport.
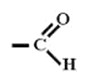
A baloldali molekulaképen a metanal (formaldehid) látható, amely mindössze egyetlen "plusz hidrogénnel" tér el a jobboldalon látható aldehid csoporttól.
Az aldehidek képezik az oxovegyületek
egyik csoportját.
Nevüket a genfi nómenklatúra szerint az "al" végződéssel jelölik,
pl. HCHO = metanal (formaldehid), H3CCHO
= etanal (acetaldehid), bár a gyakorlatban inkább a zárójelbe tett triviális neveket használják.
Előállítás
a) Elsőrendű alkoholok oxidációja
aldehideket ad:
H3C.CH2OH + O -> H3C.CHO + H2O
Sokszor a levegőben
lévő oxigén is elegendő megfelelő katalizátor
(pl platina vagy réz)
jelenlétében.
Könnyebben megy az oxidáció
krómsavval vagy vagy kénsavas
közegben mangán-dioxiddal.
Wieland kimutatta, hogy az oxidáció
tulajdonképpen dehidrogénezés, mert például palládium
oxigén nélkül is elvonja az alkohol
hidrogénjét:
H3C.CH2OH -> H3C.CHO + H2
b) Sav-kloridok redukciója
hidrogénnel palládium
katalizátor jelenlétében
aldehidet ad:
CnH2n+1COCl + H2 -> CnH2n+1CHO
+ HCl
Ez igazolja az aldehidek szerkezetét is.
c) Karbonsavak sói
kalcium-formiáttal
desztillálva aldehidet
adnak:
(C3H7)2Ca + Ca(HCOO)2 -> 2 C3H7CHO
+ 2 CaCO3
Már a savak gőzének elegye
is aldehidet ad, ha megfelelő katalizátor
(pl. TiO2) fölött vezetik el a gőzöket
300 °C körül.
Cinkpor is hasonlóan hat.
d) Alkil-magnézium-halogenidek hangyasavészterekkel aldehidet adnak:
HCOOC2H5 + C2H5MgBr -> OCH.C2H5 + C2H5OMgBr
Fizikai és kémiai tulajdonságok
A formaldehid szobahőmérsékleten
szúrós szagú gáz,
Az acetaldehid szobahőmérsékleten
forró (fp. 20,8 °C)
folyadék.
A következő tagok forráspontja
egyre inkább emelkedik, illatuk kellemes.
Igen reakcióképesek, könnyen polimerizálódnak,
vagy oxidálódnak.
Már ultraibolya sugarakkal megvilágítva bomlanak,
szén-monoxid távozással, szénhidrogénekké.
A karbonil csoport általában könnyen
reagál.
Az aldehidek kémiai reakciói közül az alábbiakat kell megemlíteni:
a) Hidrogénnel katalizátor jelenlétében alkohollá redukálhatók:
CnH2n+1CHO + H2 -> CnH2n+1CH2OH
b) Oxidáció könnyen savakká alakítja
az aldehideket. Már levegőn is oxigént
vesznek fel, előbb addíciós termék keletkezik, majd egy második aldehid
molekulához csatlakozva karbonsav:
CnH2n+1CHO + O2 -> CnH2n+1CHO.O2
CnH2n+1CHO.O2 + CnH2n+1CHO
-> 2 CnH2n+1COOH
c) Alkoholokkal az aldehidek
vízmentes ásványi savak
jelenlétében kettős étereket, úgynevezett
acetálokat alkotnak:
CnH2n+1CHO + 2 HOC2H5 -> CnH2n+1CH(OC2H5)2
+ H2O
Az acetálok kellemes virágillatúak, bor erjedésekor is keletkeznek.
Előfordulás
A nagyobb szénatomszámú aldehidek egészen 12 szénatomig,
bizonyos növények olajában, pl. citrom- és rózsaolajban fordulnak elő.
Felhasználás
Kellemes illatuk miatt illatszerekhez
használják őket.
Az egyes aldehideknél megtalálhatók a konkrét alkalmazások.
A lexikonom Szójegyzékében az aldehidek keresőszó beírásával
a kapcsolódó címszavak legyűjthetők.
Részletesebb információ található a következő aldehidekről:
formaldehid, acetaldehid,
akrolein, klorál
(triklór-acetaldehid).
Néhány aromás aldehid is megtalálható:
furfurol (furán-aldehid), ánizsaldehid
(p-metoxi-benzaldehid), benzaldehid,
fahéjaldehid, vanilin
(3-metoxi-4-oxi-benzaldehid).
Felhasznált irodalom
 Ha egy szénhidrogén
szélső szénatomján két hidrogént hidroxilgyökkel
helyettesítünk, akkor a keletkező geminális kétértékű alkoholok
nem állandóak, hanem víz lehasadásával aldehidekké
alakulnak, ezekben végső helyzetű -HC=O gyök
van.
Ha egy szénhidrogén
szélső szénatomján két hidrogént hidroxilgyökkel
helyettesítünk, akkor a keletkező geminális kétértékű alkoholok
nem állandóak, hanem víz lehasadásával aldehidekké
alakulnak, ezekben végső helyzetű -HC=O gyök
van. 
