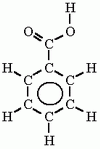
 C6H5COOH
C6H5COOHA legegyszerűbb aromás karbonsav.
benzoesav
(benzolkarbolsav, benzoát, nátrium-benzoát, E211)
 C6H5COOH
C6H5COOH
A legegyszerűbb aromás karbonsav.
Előfordulás
Növényi balzsamokban és a benzoegyantában fordul elő, az utóbbiban észter
alakjában.
A hippursav vagy benzoil-glikol vizeletben, főleg ló- és marhavizeletben található.
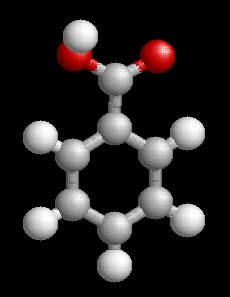
A benzoesav molekulaképe balra golyó és pálcika jobbra térkitöltéses megjelenítésben.
|

|
A Benzoesa.pdb koordináta fájl térben megjeleníthető a https://sourceforge.net/projects/openrasmol/ címről letölthető molekulamegjelenítő programmal
Előállítás:
a) Toluol vagy más, alifás oldalláncot tartalmazó aromás vegyület oxidációjával:
C6H5CH3 + 3 O2 -> C6H5COOH + 2 H2O
Hasonló eredményt ad a benzilalkohol oxidációja is.
b) Bróm-benzol és klór-szénsavas-etilészter ekvimolekuláris elegye nátriummal hevítve benzoesavas etilészterré alakul:
C6H5Br + 2 Na + ClCOOC2H5 -> C6H5COOC2H5 + NaCl + NaBr
c) Fenil-magnézium-bromidból száraz szén-dioxiddal addíciós termék keletkezik, amely vízzel elszappanosítható:
C6H5MgCl + CO2 -> C6H5COOMgCl -> (H2O) -> C6H5COOH + MgClOH
Fizikai és kémiai tulajdonságai
Fehér, kristályos
anyag.
Olvadáspontja
121°C
Forráspontja
249°C
Sűrűsége 1,32 g/cm3.
Vízben jól oldható,
alkoholban és éterben
méginkább.
Vízgőzzel desztillálható.
Az ecetsavnál erősebb sav.
Sóit és észtereit
benzoátoknak nevezik
 Felhasználás
Felhasználás
Színezék szintézisekhez
és más szerves kémiai
reakciókhoz használatos.
Nátriumsóját (nátrium-benzoát)
élelmiszerek konzerválására használják (E211).
Származékai között fontos vegyületek vannak, közülük külön megtalálhatók:
benzoil-klorid, benzamid,
benzoesavészterek