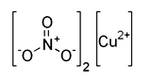
 Cu(NO3)2.3H2O
Cu(NO3)2.3H2O
A réz salétromsavval alkotott sója.
Más, 6 és 9 molekula kristályvizet tartalmazó és kristályvízmentes formája is ismert.
réz(II)-nitrát
(gerhardit)
 Cu(NO3)2.3H2O
Cu(NO3)2.3H2O
A réz salétromsavval
alkotott sója.
Más, 6 és 9 molekula kristályvizet tartalmazó és kristályvízmentes formája is ismert.
Előfordulás
A természetben, bázisos réz(II)-nitrát megtalálható a ritka gerhardit ásvány foprmájában.
 Fizikai és kémiai tulajdonságok
Fizikai és kémiai tulajdonságok
Kék, elfolyósodó, szilárd anyag.
Sűrűsége 2,32 g/cm3
Olvadáspont: 114,5°C
Melegítéskor könnyen bomlik réz(II)-oxidra, nitrogén-dioxidra és oxigénre.
A kristályvízmentes forma melegítéskor szublimál, jelezve, hogy jelentősen kovalens.
Vízben nagyon jól oldódik.
A vizes oldatából 25 °C fölött a trihidrátja, ez alatt a hexahidrátja kristályosodik ki.
Oldható metanolban és etanolban is.
Erős oxidálószer.
Ammóniával komplex vegyületeket, aminokat képez. Ezek közül a hexaamin a legstabilabb, aminek a vizes oldata sötétkék színű.
Előállítás
Réz és salétromsav reakciójával
3Cu + 8 HNO3 → 2 NO + 4H2O + 3 Cu(NO3)2
Réz(II)-oxid vagy réz(II)-karbonát és híg salétromsavval reakciójával, és a keletkezett oldat kristályosításával.
CuO + 2 HNO3 → 3 Cu(NO3)2 + H2O
A vízmentes forma előállítható rezet reagáltatva nitrogén-dioxid etil-etanoátos oldatával
Felhasználás
Más rézvegyületek előállítására.
A galvanotechnikában.
Fa pácolására.
Réz feketére színezésére.
Tűzijátékok készítésénél oxidálószerként.