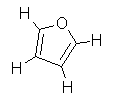
 C4H4O
C4H4Ofurán
(1,4-epoxi-1,3-butadién; divinilén-oxid)
 C4H4O
C4H4O
Egy öttagú heteroatomos (oxigén
tartalmú) gyűrűből
álló vegyület.
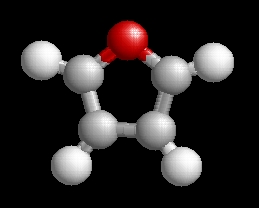
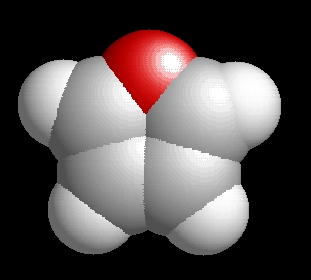
A furán molekulaképe balra golyó és pálcika jobbra térkitöltéses megjelenítésben.
|
|
A Furan.pdb koordináta fájl térben megjeleníthető a https://sourceforge.net/projects/openrasmol/ címről letölthető molekulamegjelenítő programmal.
Történet
Régóta ismert. 1870-ben állította elő Limpricht.
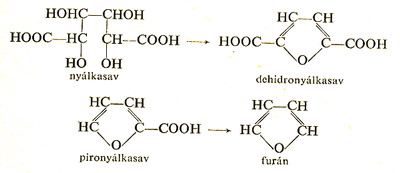
D-galaktózt tömény salétromsavval oxidálva tetraoxi-adipinsav (nyálkasav), ebből
tömény sósavval főzve víz lehasadása közben furán-2,5-dikarbonsav (dehidronyálkasav),
amely hevítve szén-dioxid lehasadásával furán-1-karbonsav (pironyálkasav) keletkezik.
Ennek bárium-sója nátromésszel hevítve furánná alakul.
Fizikai és kémiai tulajdonságai
Színtelen folyadék.
Éghető.
Olvadáspont: -85°C
Forráspont: 31,4°C
Sűrűség: 0,936 g/cm3
Lobbanáspont: -50°C
Vízben nem oldódik,
sok szerves oldószerben igen.
A származékok elnevezésének megkönnyítése érdekében a szénatomokat az oxigénatomtól
kezdődően számozzák.
Sok tekintetben aromás jellegű, de a konjugált kettős kötés hatása is jelentkezik.
Csak nehezen redukálható, katalitikus reakcióval közvetlenül tetrahidrofurán
keletkezik.
Sokféle szubsztitúciós reakcióra képes.
Pl. tömény salétromsav és ecetsavanhidrid elegyével nitrálva 2-nitrofurán keletkezik.
(Magasabb hőmérsékleten a gyűrű is felhasad.)
Szulfonálni is lehet kén-trioxiddal, dioxános oldatban savszármazékká alakul.
Halogénekkel különböző halogénezett
furánok keletkeznek, amelyek nehezen választhatók szét.
Előállítás
Iparilag furfurolból, a furán
aldehidszármazékából állítják elő.
Furfurolgőzt és vízgőzt átáramoltatva, 400°C-on, megfelelő katalizátoron.
Felhasználás
Gyógyszerek, és műanyagok előállításának
alapanyaga.